
盘点 | 全球免疫细胞疗法现状分析
发布时间:2024-08-26
免疫细胞治疗被认为是继手术、放疗和化疗之后的第四大肿瘤治疗技术。
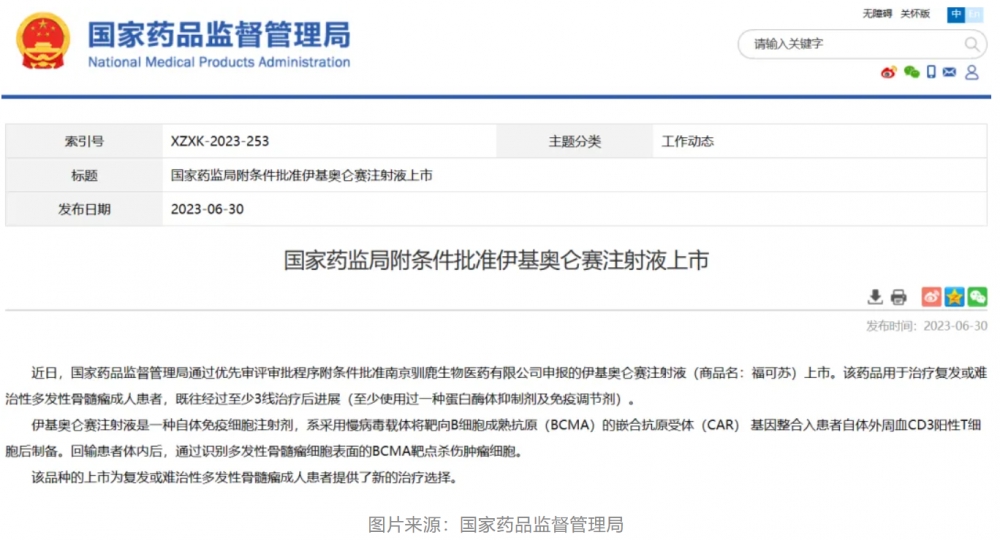
2023年6月30日,国家药监局批准伊基奥仑赛注射液(商品名:福可苏)上市,用于治疗复发或难治性多发性骨髓瘤成人患者,这是国内首款靶向BCMA(B细胞成熟抗原)的CAR-T产品,也是我国上市的第三款免疫细胞治疗产品,意味着将有更多的肿瘤患者因此获益。
01.
免疫疗法全球研发现状
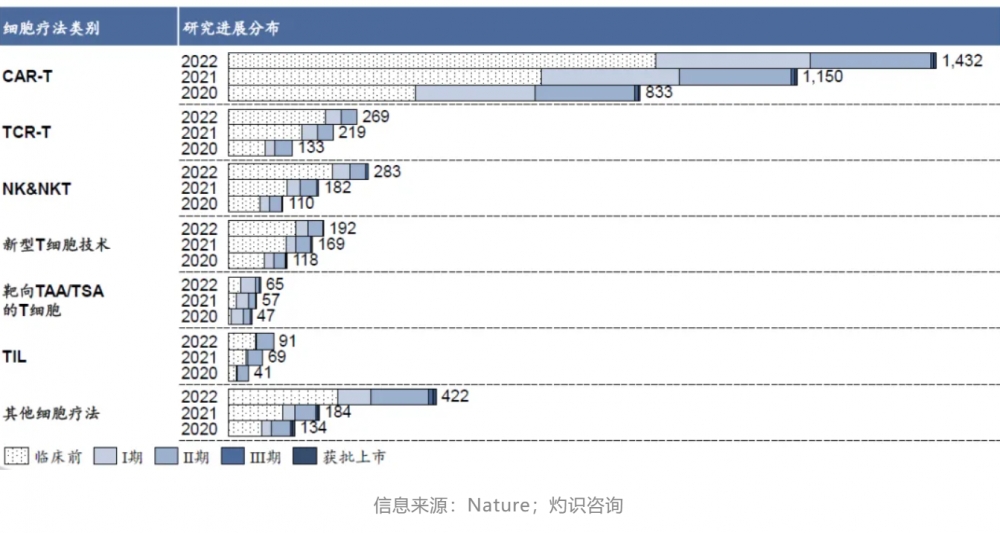
截至2023年6月底,全球经批准上市的免疫细胞治疗产品共15款,包括CAR-T细胞产品10款,DC细胞产品3款,CIK细胞产品和T淋巴细胞产品各1款。可以看出,上市的免疫细胞产品以CAR-T疗法为主,适应症均为血液系统恶性肿瘤,其中7款以CD19为靶点,3款以BCMA为靶点。我国药监局共批准3款CAR-T疗法上市,适应症为大B细胞淋巴瘤和多发性骨髓瘤。
全球上市的免疫细胞产品
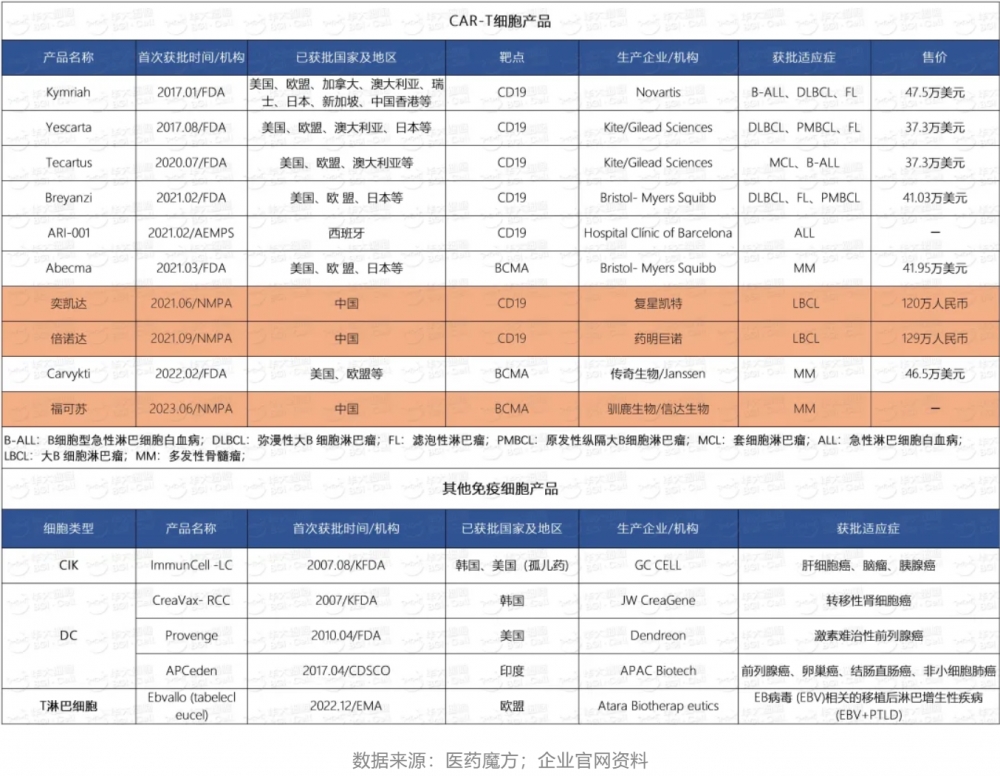
另外,据相关报道,中国台湾卫生主管部门已批准四家可进行自体免疫细胞治疗的医院,提供治疗项目包括CIK、NK、DC、DC-CIK等。
自国家药监局在2017年发布《细胞制品研究与评价技术指导原则(试行)》以来,免疫细胞治疗产品纳入药品管理体系的监管路径已十分清晰(作为医疗技术目前仅允许医疗机构开展临床研究,尚不可进行临床应用)。据不完全统计,通过国家药监局临床试验默示许可的免疫细胞疗法IND达80余种,进入百花齐放、百家争鸣的时代。
免疫细胞技术多样化:除已经上市的CAR-T细胞产品,在研的免疫细胞技术包含NK、CIK、TIL、DC等,比如华大吉诺因开发“靶向新生抗原自体免疫T细胞注射液”,正在开展治疗晚期实体瘤患者的临床试验。(点击了解详情)
探索更多临床适应症:虽然血液系统恶性肿瘤仍是重点研发领域,但更多的适应症在探索之中,包括卵巢癌、肝细胞癌、肾癌等实体肿瘤以及自身免疫系统疾病等,如已上市产品倍诺达新增适应症“中重度难治性系统性红斑狼疮”IND已获批。
拓展多元化支付路径:免疫细胞治疗产品上市之初,以120万一针“抗癌神药”被热议,随着企业、政府、商业保险、慈善基金等各方协作推动,拓展了多种创新支付方式,如上市产品奕凯达已纳入平安人寿、泰康在线等60多款商业健康保险以及上海沪惠保、北京京惠保等80多款城市“惠民保”。
美国生物学家George Daley曾说过:“如果20世纪是药物治疗的时代,那么21世纪将是细胞治疗的时代”。免疫细胞疗法作为一种迅速崛起的治疗方法,已经在多种癌症治疗上展示出强大的治疗效果,随着技术的不断进步和临床实践的积累,免疫细胞疗法在未来有望实现更加个体化、精准化和高效化的治疗,惠及更多的患者。
详情咨询 请致电:400-062-0045
