细胞治疗,一般是指利用生物工程等方法对事先获取的正常人体细胞进行处理,使某些特定类群的细胞具有更强的免疫杀伤能力或促进组织修复等特殊功能,再经过体外培养扩增后,最终将细胞移植到患者体内,从而达到治疗或缓解疾病的目的。
根据国家药品监督管理局食品药品审核查验中心(CFDI)2019年11月28日发布的《GMP附录-细胞治疗产品》(征求意见稿),细胞治疗产品是指:人源的活细胞产品,包括由细胞系,以及来源于自体或异体的免疫细胞、干细胞和组织细胞等生产的产品,不包括输血用的血液成分、已有规定的造血干细胞移植,生殖相关细胞,以及由细胞组成的组织、器官类产品等。
在多种重大疾病的治疗或缓解中,细胞治疗发挥了越来越重要的作用。免疫细胞疗法也是继手术、放疗、化疗和靶向治疗之后的最新一代抗癌利器,干细胞疗法也在多种组织器官再生中取得了不断突破。进入21世纪以来,全球细胞治疗产业开始了加速发展,至今已有数十种细胞治疗产品获得批准,主要分布于美国、韩国、欧盟、日本、台湾、印度等国家和地区,其中多数为间充质干细胞(MSCs)疗法等干细胞治疗产品,也包括2款嵌合抗原受体T细胞(CAR-T)疗法等免疫细胞疗法和软骨细胞组织工程产品等其他类型的细胞治疗产品。我们将分三期专题向大家介绍免疫细胞治疗产品、干细胞治疗产品与组织工程产品。本期专题我们首先介绍免疫细胞产品。
2010年5月,来自美国宾州的5岁小女孩Emily Whitehead被诊断出患有急性淋巴细胞白血病(acute lymphoblastic leukemia, ALL)。ALL是一种儿童多发性白血病,占儿童白血病的70%以上。ALL是进展最快的癌症之一,原始的B细胞会在血液里疯狂增殖,进而侵犯到肝脏、大脑等器官。虽然高强度化疗可以治疗约85%的儿童患者,但是副作用很大。在接受两轮化疗后,Emily的病情出现短暂的缓解,不过2011年10月病情又复发并逐渐恶化。Emily申请了骨髓移植,这是她最后的希望。Whiteheads一家人和Carl June教授(左二)在2016年的Parker研究所癌症免疫疗法启动晚宴上 图片来源 | parkerici2012年3月,父母带Emily来到了费城儿童医院,当时她体内几乎每个器官都有肿瘤细胞浸润,危在旦夕。恰巧宾夕法尼亚大学医学院正在这里开展一种“活的”药物——CAR-T治疗——的早期临床试验,尽管只有三位成人患者参与,Emily还是接受了治疗。医生们先把Emily体内的免疫细胞提取出来,向这些免疫细胞里导入一个可以识别癌细胞的系统,再把这些免疫细胞回输到Emily体内。在Emily接受第三次注射后,她出现了严重细胞因子风暴带来的高烧、呼吸衰竭和休克,命悬一线,活过这个晚上的可能性微乎其微。千钧一发之际,当时的CAR-T项目负责人Carl June教授紧急申请了一种刚刚上市的药物,靶向白介素-6的抗体,为Emily缓解严重的副作用。奇迹发生了,14天后,在Emily 7岁生日那天,她从休克中醒了过来,身体状态迅速恢复。随后的检测结果显示,Emily体内的白血病细胞都不见了,而免疫细胞还在,Emily死里逃生。更令人惊喜的是,如今8年过去了,Emily的白血病再也没有复发。随着Emily和CAR-T的神奇故事被越来越多的人们了解,她也成了美国的抗癌明星,通过她的基金会帮助其他儿童癌症患者抗击癌症。这就是CAR-T治愈儿童白血病的第一个案例。
Kymriah和Yescarta
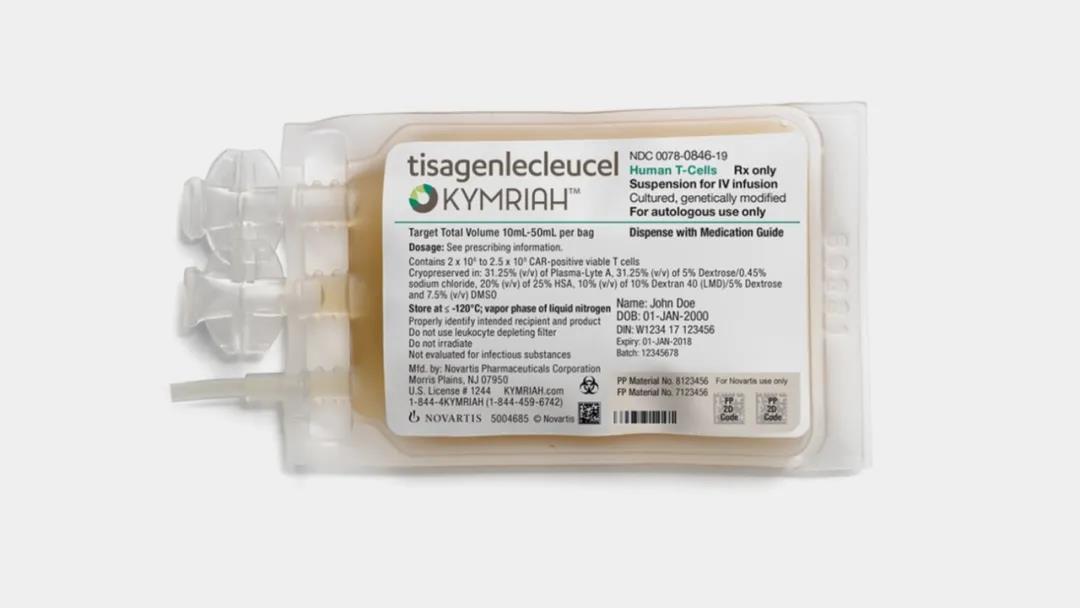
Emily的成功案例为Carl June教授带来了大量支持。Carl June教授是美国著名免疫学家和肿瘤学家,也是免疫细胞治疗领域的奠基人。Carl June教授团队开发的这种专门治疗ALL的方案,CAR-T免疫细胞疗法,由诺华制药(Novartis)推向市场(BL 125646),商品名为Kymriah。2017年8月30日美国食品药品管理局(Food and Drug Administration,FDA)正式批准了Kymriah上市,用于治疗25岁以下化疗无效或复发性儿童和青少年ALL患者。2018年美国FDA又批准了Kymriah用于治疗在经过两次或更多全身治疗方案后无响应的成人复发或难治性大B细胞淋巴瘤,包括未另作说明的弥漫性大B细胞淋巴瘤(DLBCL),高级别B细胞淋巴瘤和滤泡性淋巴瘤引起的DLBCL。2018年Kymriah分别在欧盟和加拿大获批,2019年在日本获批用于ALL的治疗。
Kymriah 图片来源 | fiercepharma
2017年10月18日,风筝制药(Kite Pharma,已被吉利德Gilead收购)开发的Yescarta成为获得美国FDA批准上市的第二种CAR-T疗法(BL125643)。Yescarta用于治疗经过两次或更多全身治疗后的成人复发或难治性大B细胞淋巴瘤,包括未另行指明的弥漫性大B细胞淋巴瘤(DLBCL),原发性纵隔大B细胞淋巴瘤,高级别B细胞淋巴瘤和滤泡性淋巴瘤引起的DLBCL。
癌症免疫疗法是一种利用患者自身免疫系统识别并杀死癌细胞,从而治疗和缓解癌症的方法,也是细胞疗法重要的研究和临床应用方向,其中以CAR-T为代表的免疫细胞疗法是近年来进展最迅速的领域之一。CAR-T全名为嵌合抗原受体T细胞,医生首先获取患者自身的T细胞,通过基因工程技术给T细胞加上能识别癌细胞表面特异蛋白并同时激活T细胞的嵌合抗原受体(Chimeric antigen receptor, CAR),将T细胞打造为可以精准识别和攻击癌细胞的强力武器。经过在体外培养和大量扩增,再将CAR-T细胞回输到患者体内,最后监控T细胞治疗的效果。CAR-T免疫细胞疗法是抗击癌症的革命性疗法,尤其是治疗晚期血液癌症的里程碑式技术,为许多面临有限治疗选择的患者带来了新的希望。Kymriah和Yescarta两款CAR-T疗法都靶向B细胞表面的CD19,Kymriah治疗B细胞急性淋巴性白血病具有83%的缓解率,Yescarta治疗B细胞非霍奇金淋巴瘤也达到了72%的缓解率。Yescarta治疗儿童ALL的12个月生存率高达79%,其中有不少患者达到了完全缓解和治愈,而全球首例接受治疗的白血病成人患者Bill Ludwig已经实现了9年无癌生存。已有约1800名血液癌症患者接受了Yescarta治疗,美国血液学会的数据显示,接受Yescarta治疗的淋巴瘤患者中,有近半数在一次治疗后存活了至少3年。在101位接受Yescarta治疗的难治性大B细胞淋巴瘤患者中,有47位至少存活了3年。全球数百项正在进行的临床试验结果表明,靶向CD19以外其它靶点,例如CD22的CAR-T疗法也可以获得较高的缓解率。CAR-T疗法从最初的第一代到第二代再到目前的第三代,对癌细胞的识别能力和整体安全性也在不断提升。除了血液癌症以外,还有大量临床研究正在探索CAR-T免疫细胞疗法在治疗实体肿瘤中的作用[1]。自2017年首次获批以来,CAR-T疗法的临床研究和开发出现了爆发式的增长,例如来自杨森(Janssen)/南京传奇、BMS、吉利德/KitePharma、Juno Therapeutics,Celgene,Bluebird Bio,Mustang Bio,Servier,Pfizer,Cellectis,Celyad和诸多中国生物医药公司开发的CAR-T疗法都有不错的成绩,今年可能至少会有2款CAR-T疗法获得美国FDA批准。目前中国已有20多家企业的超过30款CAR-T产品获得IND受理,除Yescarta与Kymriah外已有十几种CAR-T疗法获得了临床批件,距离上市近在咫尺。
CAR-T不是一种普通药物,而是细胞制品。作为一种“活的”药物,CAR-T疗法的步骤比普通药物要复杂得多。通常情况下,CAR-T治疗包括分离、修饰、扩增、回输、监控几个阶段,是一种个性化的治疗方案。CAR-T疗法的最大优势在于精准攻击癌细胞,和放疗、化疗相比,对其他组织的损伤较小,同时回输的T细胞还能在患者体内存在几个月的时间,继续杀伤新出现的癌细胞。
CAR-T疗法的局限性有以下几种:
安全性:大量T细胞回输会造成细胞因子风暴,也是引起Emily高烧和休克的原因,非常危险[2];
副作用:具有潜在的脱靶效应,产生一定的副作用;
适应症有限:目前CAR-T疗法的适应症绝大部分都是血液癌症,治疗实体瘤的效果还有待提高;
患者存在一定的复发风险[2];
生产制备工艺复杂,价格非常昂贵:目前的技术只能实现单人单次制备、无法大规模生产,导致了CAR-T细胞价格较高等问题,Kymriah在美国的定价为47.5万美元,Yescarta在美国的定价为37.3万美元,CAR-T疗法的总费用至少为75万美元,其中非药品的住院费用和护理等费用为40万美元至45万美元,解决大规模生产难题,降低成本是未来的趋势。
除了以上几个方面,患者T细胞数量不足和患者入选合格率低等问题也限制了CAR-T疗法的临床应用。如果能在健康的时候预先储存自己的免疫细胞,就可以为将来有可能接受的免疫细胞治疗提供充足的细胞,降低细胞数量不足的风险。
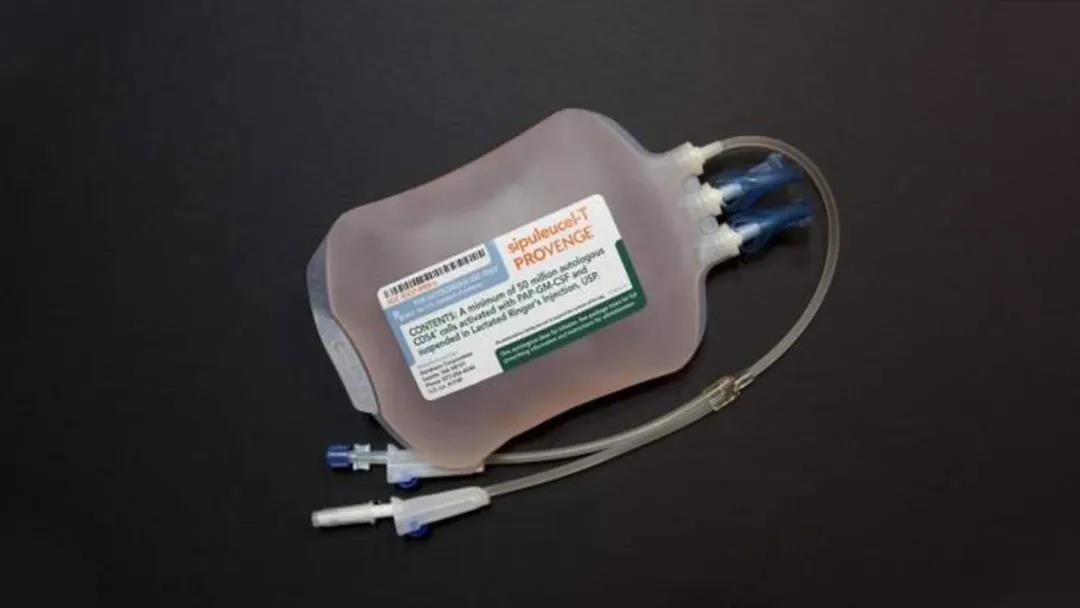
免疫细胞疗法不仅有CAR-T一种,许多其他种类的免疫细胞也可以用于免疫细胞治疗。从2007年韩国食品药品安全部(Ministry of Food and DrugSafety,MFDS)批准第一款免疫细胞治疗产品Immuncell-LC至今,全球获批上市的免疫细胞治疗产品共有12种,除了前面提到的2款CAR-T疗法以外,另外10种基于T细胞、树突细胞等类型细胞的抗癌免疫细胞治疗产品主要用于治疗实体肿瘤等疾病。Provenge 图片来源 | clinicaltrialsarena
例如2010年上市的PROVENGE是第一个在美国被批准用于癌症治疗的疫苗,用于治疗无症状或症状轻微的转移性去势抵抗性前列腺癌(BL 125197)。PROVENGE是美国FDA批准的唯一一种由患者自身免疫细胞制成的前列腺癌免疫疗法,开创了癌症免疫治疗的新时代。目前已有超过3万名男性患者接受了PROVENGE治疗,PROVENGE在临床上已被证明可以延长晚期前列腺癌患者的生命。2019年我国台湾地区4家医院与3家公司合作开展的细胞因子诱导杀伤细胞(Cytokone-Induced Killer cell, CIK)与树突细胞(Dendritic Cell, DC)自体细胞免疫疗法陆续获得批准,用于白血病和多种实体瘤的治疗,预计今后将有更多的医院与公司开发的免疫细胞疗法获批。
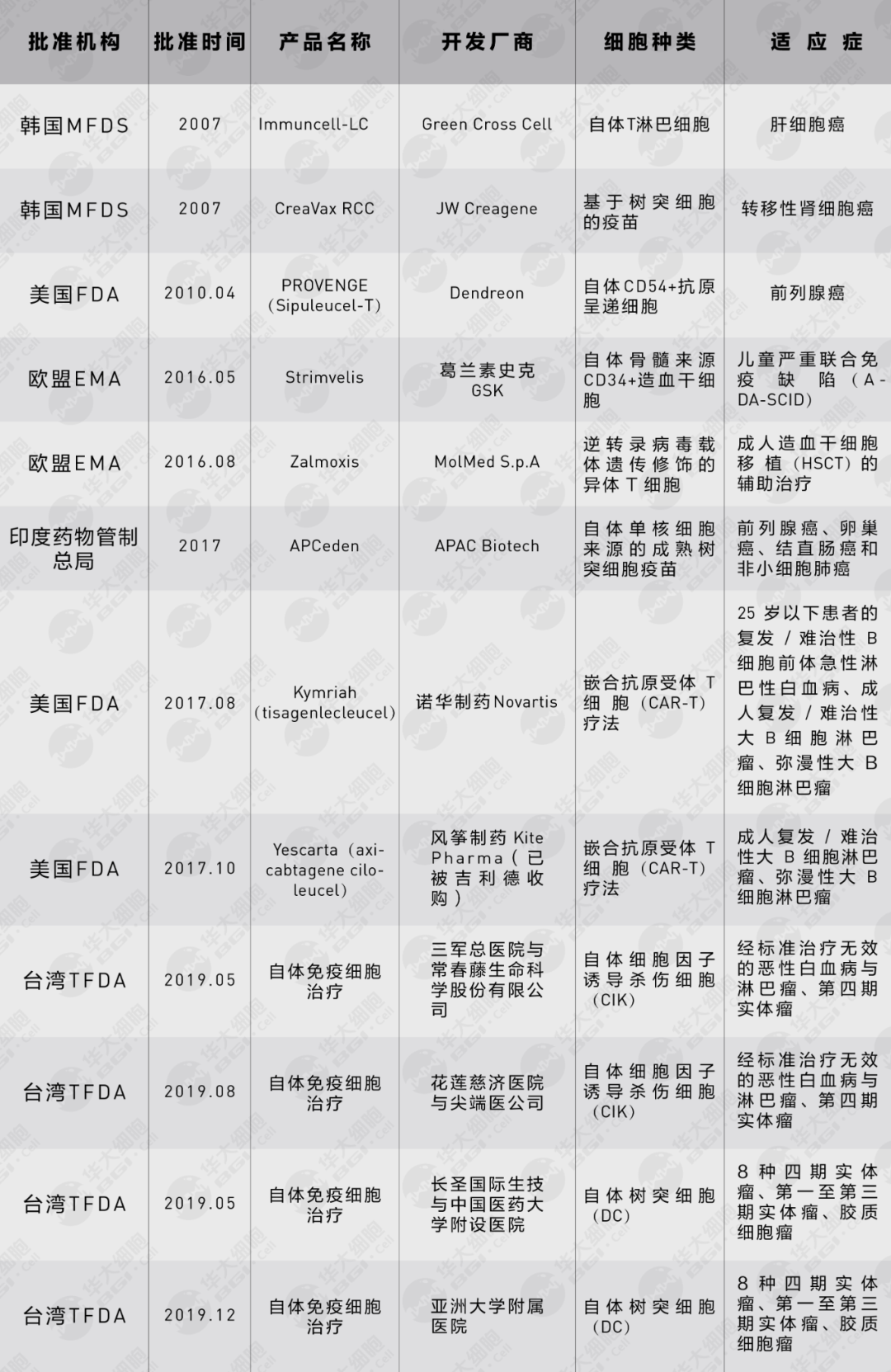
目前全球有数百个免疫细胞治疗相关的临床研究正在进行,除了占大多数的CAR-T疗法以外,还有T细胞受体嵌合型T细胞疗法(TCR-T)和肿瘤浸润淋巴细胞(TIL)疗法等多种基于T细胞、自然杀伤(NK)细胞、巨噬细胞等免疫细胞的临床研究[2],适应症不仅有血液癌症,还有多种组织和器官的实体肿瘤,未来几年内免疫细胞治疗产品的上市有望迎来爆发式增长,为成千上万患者们提供更多可能拯救生命的选择。
参考文献
1. Schultz, L. and C. Mackall, Driving CAR T cell translation forward. Sci Transl Med 11, (2019) DOI: 10.1126/scitranslmed.aaw2127.
2. June, C.H. et al., CAR T cell immunotherapy for human cancer. Science 359, 1361-1365 (2018) DOI: 10.1126/science.aar6711.
[3] Siddhartha Mukherjee. The Promise and Price of Cellular Therapies. The New Yorker. July 22, 2019.
[4]张小欣,王煜全. 创新地图|CAR-T癌症免疫疗法的进展和挑战. 全球创新260讲. 2017.10.15.
[5]王立铭. 免疫疗法(下):如何戳破癌细胞的伪装?众病之王的解决方案. 2018.12.02.
[6] emilywhiteheadfoundation.org/
[7] www.parkerici.org/the-latest/from-leukemia-to-cancer-free-how-car-t-immunotherapy-saved-emily-whitehead/
[8] www.fda.gov/home
[9] www.ema.europa.eu/en
[10] www.mfds.go.kr/eng/index.do